・反応熱はkJで表し,エネルギーであることを説明する。 ・発熱反応と吸熱反応の2つの例をあげ,エネルギーの放出と吸収を図に表す。 ・化学反応式を復習させながら,反応熱について触れる。 ・kJとkJ/molの違いについて説明する。 · 反応後の物質の化学エネルギーが高い場合は、 その分周りから 熱エネルギーを吸収し化学エネルギーに変えているので吸熱反応 となります。 最後に、吸熱反応、発熱反応の例を挙げておき発熱反応で 熱 q が生じると、この熱は周囲に「乱雑さ」をばらまき、周囲のエントロピーを増加させます。 そのため通常は 発熱反応 (ΔH < 0) が起こりやすいのですが、0 °C 以上における 氷の融解のように、自発的に生じる吸熱反応もあります。これは系
受験化学 24 エネルギー図 みかみの参考書ブログ
発熱反応 吸熱反応 例
発熱反応 吸熱反応 例-・ 発熱反応と吸熱反応 化学反応に伴って、発生または吸収される熱量を反応熱と呼ぶ。すべての物質は、固有のエネルギー(化学エネルギー)を持っている。化学反応が起こり、反応物が生成物に変化すると反応物が持っているエネルギーと生成物が持っているエネルギーとの差が、反応熱として現れることになる。 熱を発生する反応を発熱反応、熱を吸収する反応を吸熱反応と呼ぶ。(化学:物 · 化学反応は実験室で起こるだけでなく、私たちの体内でも日常的に起こります。 例えば、角氷の融解または液体水の蒸発は吸熱反応であり、一方、水が角氷に凍結する場合、それは発熱反応と呼ばれます。 化学反応中には、分子を結合する結合に存在する多くのエネルギー要件があります。 そのため、分子と化合物(反応物)の間で反応が起こると、結合が破壊さ



3 1tabc Hkh Left 1right Lihat Cara Penyelesaian Di Qanda
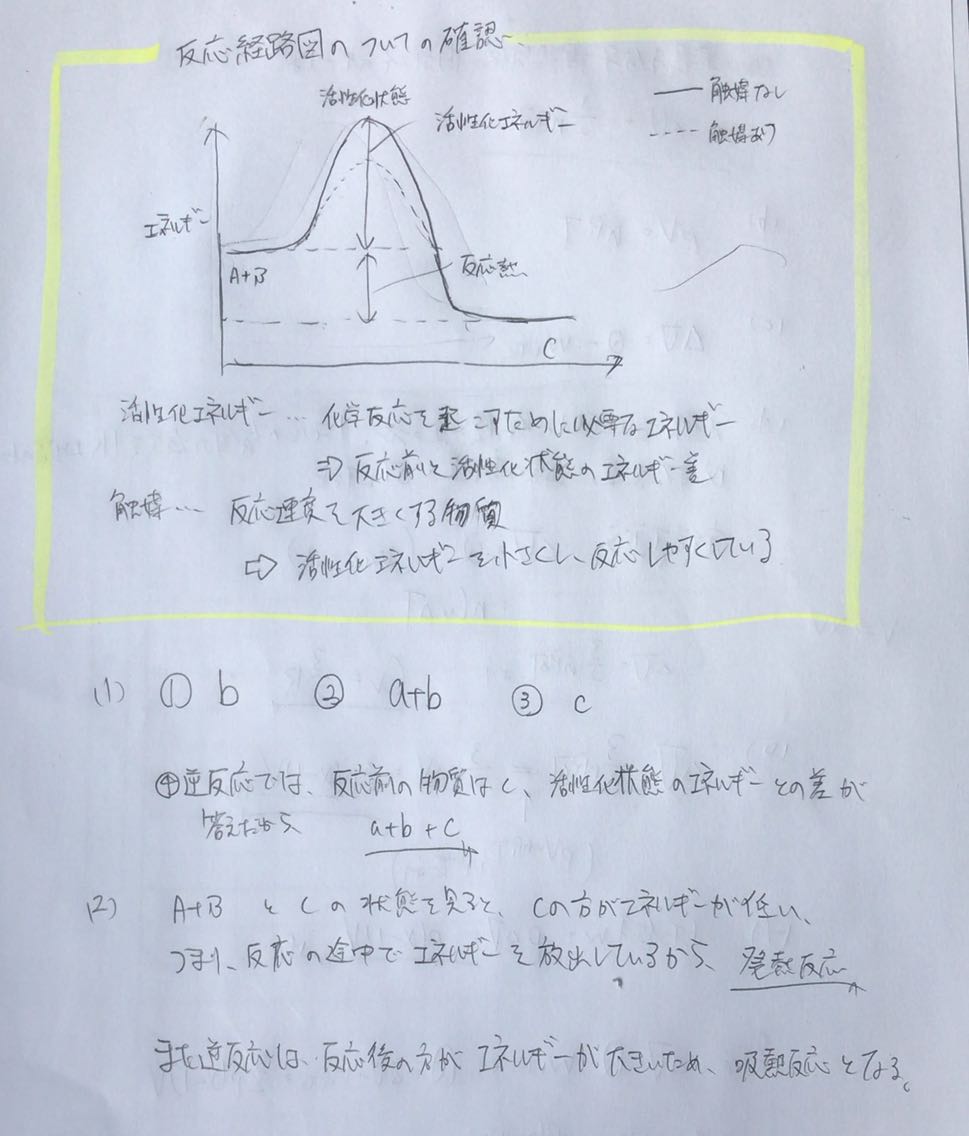
熱の吸収をともなう反応を吸熱反応,熱の発生をともなう反応を発熱反応と定義する. 発熱反応では,系の温度を一定に保つために熱エネルギーを外界へ移動させる必要があるので, は負の値となる. 吸熱反応では,その逆である. すなわち, である. なお,反応を標準状態で行わせたときの反応エンタルピーを と書く.B発熱反応と吸熱反応 化学反応に伴い,発生または吸収する熱量を反応熱という。 化学反応において,反応物の持つ内部エネルギーの総和が生成物の内部エネルギ ーの総和より大きいと余分なエネルギーが放出されながら進む。このように反応熱発熱反応 吸熱反応 発熱反応:化学反応が起こるとき,熱を放出(≡運動エネルギーが増加)する反応。 を例に熱化学方程式の2 つの読み方について説明します。 読み方1 右辺の反応熱(生成熱)が正
発熱反応(はつねつはんのう、英語:exothermic reaction)とは、エネルギーを系外へ熱などとして放出する化学反応のこと。 広義には相転移、溶解、混合等の物理変化も含める。 放出するエネルギーは熱だけでなく、光、電気などの形をとる場合もある。 対義語は吸熱反応。吸熱反応(きゅうねつはんのう、英語:endothermic reaction)とは、エネルギーを熱として吸収する、つまり負の反応熱を持つ化学反応のこと。 広義には相転移、溶解、混合等の物理変化(吸熱変化)も含める。 反応によっては熱でなく電気などの形でエネルギーを与えることで進行するものもある。 · 化学反応のうち、 外部に熱を放出する反応のことを 発熱反応 といいます。 発熱反応の例として挙げられるのが、カイロです。 カイロの袋の中には鉄が入っていて、その鉄が空気中の酸素と反応し、酸化鉄が生成します。
· 吸熱反応の良い例には、 塩の 溶解が含まれ ます。 食塩である必要はなく、溶媒は水である必要はありません。 水酸化バリウム八水和物結晶と乾燥塩化アンモニウムとの反応 塩化アンモニウムを水に溶かす 塩化チオニル(SOCl 2 )と硫酸コバルト(II)七水和物と の反応 水と硝酸アンモニウムの混合 水と塩化カリウムの混合 エタン酸と炭酸ナトリウムとの反応 · 吸熱反応があまり起こらない理由 吸熱反応の実験をしましたが、温度はあまり下がりません。 買った市販の瞬間冷却材を使ってみましたが、最初は氷のように冷たかったですが、3分で水と同じくらいになってしまいました。熱を放出する反応は発熱反応、吸収する反応は吸熱反応である。 たとえば、H 2 (気体)1モルがO 2 (気体)05モルと反応してH 2 O(液体)1モルが生じる反応は次のような式で表される発熱反応である。 H 2 (気) ½O 2 (気)= H 2 O(液) 286 kJ




夕凪亭別館 写真館 化学反応と熱




質量保存の法則 化学変化と熱の出入り Ict教材eboard イーボード
生成物の中の結合エネルギーが反応物質のそれより小さいとき、Qは正となり発熱反応に、逆のときQが負の値となって吸熱反応となる。水素の燃焼反応は典型的な発熱反応である。 2H 2 O 2 ―→2H 2 O578kcal すなわち1モル当り578キロカロリーの熱を発生する。実験 吸熱反応 17 9 27(水)、28(木) 普通教室 はじめに 骨のある3つの化学反応式、そして、珍しい吸熱反応の実験を行います。希望する班には、アンモニアが発生する発熱反応も行わせます。 上:指の背で触れ、冷えていることを確かめる様子 · 生成熱には発熱反応と吸熱反応の両方があります。 燃焼熱 ある「 物質1mol 」が完全燃焼するときに発生する熱量を 燃焼熱 といいます。 この反応はすべて発熱反応となります。 \( \displaystyle \mathrm{H_2 \frac{1}{2} O_2=H_2OQ'}\)




5分でわかる化学変化と熱 物質が変化する時に必ず伴う熱の出入りについて元研究員が解説 Study Z ドラゴン桜と学ぶwebマガジン



受験化学 24 エネルギー図 みかみの参考書ブログ
吸熱反応 (きゅうねつはんのう、 英語 :endothermic reaction)とは、 エネルギー を 熱 として吸収する、つまり負の 反応熱 を持つ 化学反応 のこと。 広義には 相転移 、 溶解 、混合等の 物理変化 (吸熱変化)も含める。 反応によっては熱でなく 電気 などの形でエネルギーを与えることで進行するものもある。 対義語は 発熱反応 。 吸エルゴン反応 は ギブズ吸熱反応の光合成およびその他の例 化学反応は環境との間でエネルギーをやり取りします。 吸熱反応は環境からエネルギーを吸収し、発熱反応は環境にエネルギーを伝達する 反応が吸熱性か発熱性かを決定するのは、既存の結合を切断するために供給しなければならないエネルギーと、新しいリンクが形成されたときに放出されるエネルギーとの間のバランスです発熱反応と吸熱反応が併発する完全混合型反応装置の定常状態の数およびそれらの安定 性は,両 反応の熱的特性および操作条件によって大きく変化する本研究では,発 熱反応 と吸熱反応の反応熱と反応速度定数との積の和を表す関数の形状を6種 類に分類し




今後の予定 日程変更あり 5日目 10月21日 木 小テスト 4日目までの内容 小テスト答え合わせ 質問への回答 前回の復習 Ppt Download




化学反応と熱 光 の勉強法のわからないを5分で解決 映像授業のtry It トライイット
( 吸熱反応 )熱を吸収する反応 例)発熱 メタンを完全燃焼すると熱を発生する。 吸熱 赤熱した黒鉛に水蒸気を触れさせると熱量が吸収される。 化学反応に伴って発生する,または吸収される熱量を( 反応熱 )という。 化学エネルギーと反応熱をまとめると次のようになる。 化学エネルギーの大小 エネルギー差 · 吸熱反応では融解熱や蒸発熱を例にして解説しましたね。 発熱反応は反応に伴って熱や電気、光が発生する のに対し、 吸熱反応は反応を進めるために光や電気、熱が必要になる 反応です。熱を発生する化学反応→発熱反応 (例) 2H 2 +O 2 →2H 2 O 熱を吸収する化学反応→吸熱反応 (例) C(黒鉛)+H 2 O→CO+H 2




発熱反応と吸熱反応の見分け方を教えて下さい Clear




エタノール 完全 燃焼 化学 反応 式 プログラム ニュース
発熱反応(はつねつはんのう、英語:exothermic reaction)とは、エネルギーを系外へ熱などとして放出する化学反応のこと。 広義には相転移、溶解、混合等の物理変化も含める。 放出するエネルギーは熱だけでなく、光、電気などの形をとる場合もある。 対義語は吸熱反応。発熱と吸熱反応を2つずつ紹介します。 実験1:おいしい吸熱反応(実験No4) 正確には途中で発熱反応も入るので、問題ありですが、おいしいのでのせます。 材料:重曹、クエン酸、グラニュー糖、水 重曹とクエン酸を2:1の割合で混ぜます。 そこに水をできるだけ少なく加えて型抜きします。 入浴剤の完成です。 ビーカーに水を入れて入浴剤を入れると11:発熱反応と吸熱反応 について、実験と結果を学習します。 ※無料講座の続きは、有料講座のタブでご確認できます。 応用問題の解答は、応用問題のタブでご確認できます。 If playback doesn't begin shortly, try restarting your device Videos you watch may be added to the TV



中学理科 化学反応式の作り方 問題の解き方がわかる3ステップ Qikeru 学びを楽しくわかりやすく




気体 液体 固体の間での状態変化と熱の出入り 密度や体積の関係を解説
ときの反応が発熱反応であるからである。また アルコールが水にとけるときの反応も発熱反応 である。吸熱反応の例としては食塩を水にとか したときに熱が吸収されて水温が下るなど,主 として固体塩が水にとける場合に多くあるよう である。(溶解熱) · 日常生活での反応熱(発熱・吸熱反応)の利用例を教えて下さい。 通報する この質問への回答は締め切られました。 質問の本文を隠す A 同じカテゴリの新着質問 A 回答 (2件) 最新から表示 回答順に表示 No2 · ページ 2 / 3 よぉ、桜木建二だ。今回は状態変化と反応熱の最後、「気化熱」について勉強していこう。 気化熱・蒸発熱・昇華熱は気化・蒸発・昇華と同様に紛らわしいワードだ。違いをしっかり理解しておこう。 現象の本質を理解することが大切だ。
/endergonic-vs-exergonic-609258_final-2904b2c359574dfcb65a9fca2d54179a.png)



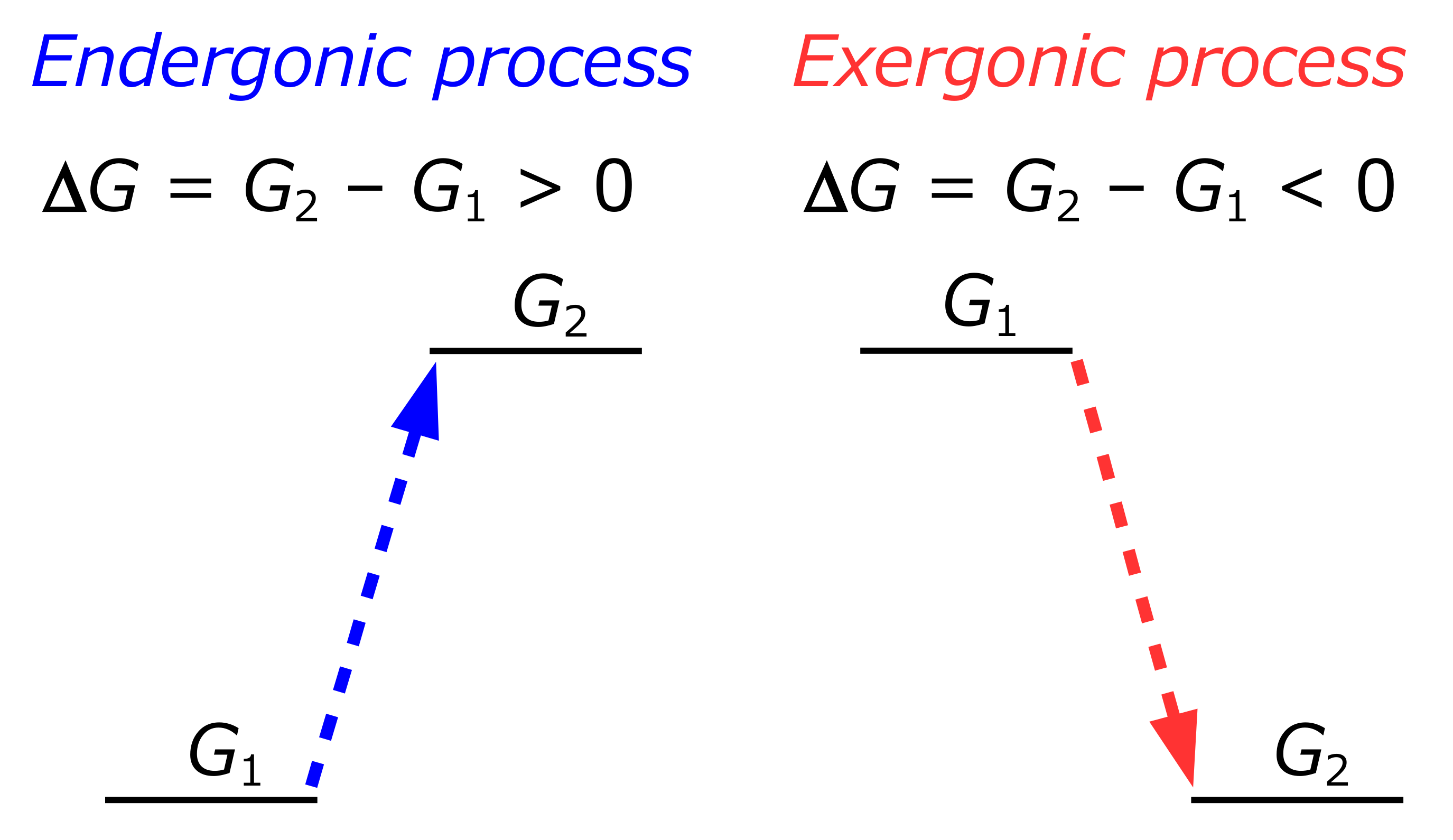
吸エルゴン反応と発エルゴン反応の違いを理解する必要があります




凝固点降下 熱化学方程式 高校生 化学のノート Clear
吸熱反応なので、反応後の右辺に『− 熱』と書かせます。 水酸化バリウム+塩化アンモニウム → 塩化バリウム+アンモニア − 熱 化学反応式は指導する必要はありませんが、私の授業では教えました。日本大百科全書(ニッポニカ) 吸熱反応の用語解説 化学反応が進行するにつれて、熱を吸収する反応をいう。これに対し、熱を発生する反応を発熱反応という。化学反応が一定の温度の下で原系から生成系へとおこる場合、反応を完結させるために外部から熱量を吸収しなければならない反応 · 吸熱反応の例 ① ~アンモニウムと を混ぜる反応 (例)塩化アンモニウムに水酸化バリウムを混ぜる 塩化アンモニウム + 水酸化バリウム → 塩化バリウム + アンモニア + 水 → ② クエン酸と を混ぜる反応 クエン酸を使っていれば吸熱反応です。




Ppt 5章 物質の三態 気体 液体 固体 と気体の法則 2 回 まず 復習 初回では 以下を紹介した 化学熱力学 三態 気体 液体 固体 外界と系 孤立系 閉じた系 開いた系 Powerpoint Presentation Id




5 9 1 1 1 2 2right 2 J Descubre Como Resolverlo En Qanda




5 9 1 1 1 2 2right 2 J Descubre Como Resolverlo En Qanda




中2理科 化学反応と熱 発熱反応と吸熱反応 Pikuu




夕凪亭別館 写真館 化学反応と熱




理科の発熱反応と吸熱反応 中学生 理科のノート Clear




水の電気分解と炭酸水素ナトリウムが吸熱反応なのはなぜですか Clear



受験化学 21 熱化学1 みかみの参考書ブログ




中2 理科 化学変化 中学生 理科のノート Clear




高校化学 発熱反応と吸熱反応 映像授業のtry It トライイット




気体 液体 固体の間での状態変化と熱の出入り 密度や体積の関係を解説




吸熱反応の意味 用法を知る Astamuse



外部条件に対する平衡の応答 平衡 圧力 温度 反応物と生成物の濃度に応じて変化する Ppt Download



化学




反応熱の計算 生成熱 燃焼熱 溶解熱 中和熱 結合エネルギー 理系ラボ




熱化学方程式の解き方 基本からわかりやすく解説 高校生向け受験応援メディア 受験のミカタ




活性化エネルギー Wikipedia




ための 化学反応式 を書く方法について考え




Wo16 0599号 化学蓄熱装置 Astamuse




発熱反応と吸熱反応 中学理科 2年 1分野 化学変化と原子 分子11 Youtube




Kelas 8 Catatan Tentang 中2 理科 発熱反応と吸熱反応 Clear




吸熱反応 Youtube




高校化学 発熱反応と吸熱反応 映像授業のtry It トライイット
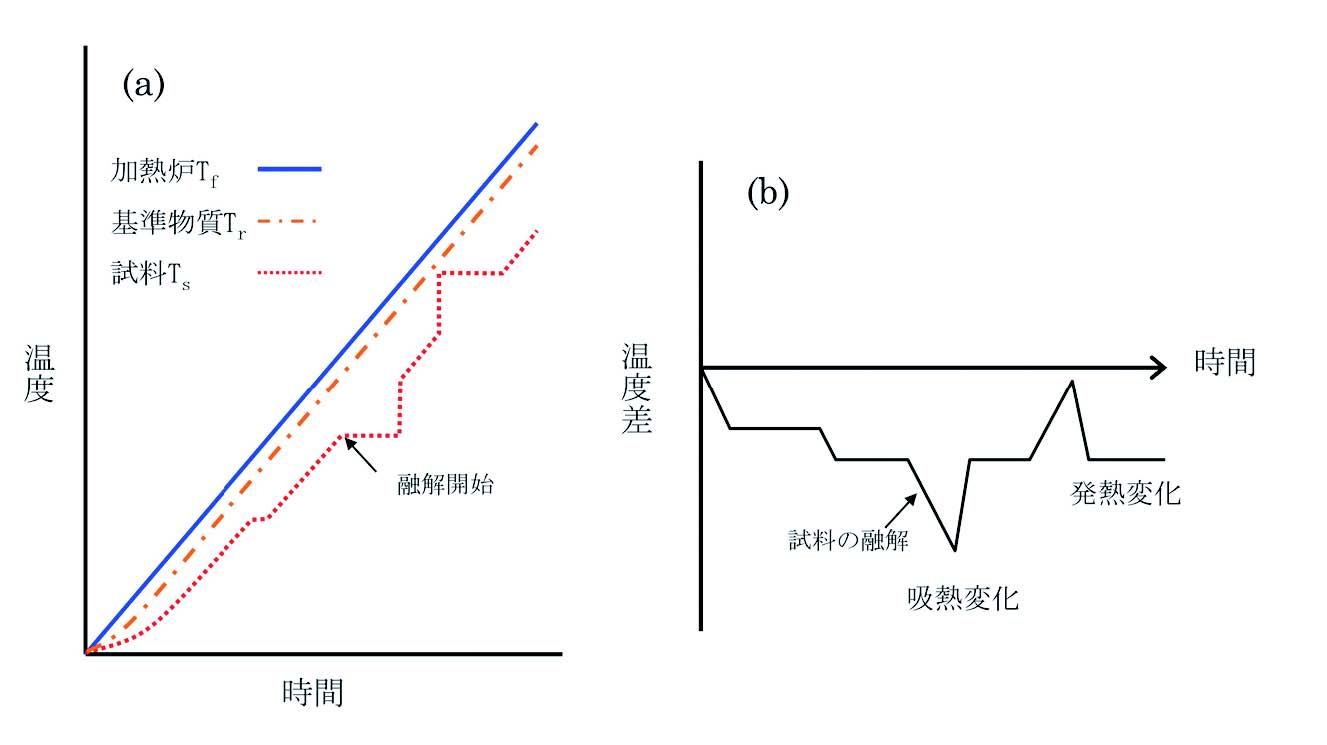



示差熱分析 Dta の原理と応用 Jaima 一般社団法人 日本分析機器工業会




化学反応式とは違うの 熱化学方程式 ヘスの法則 ル シャトリエの原理 ふかラボ




中2理科 吸熱反応 映像授業のtry It トライイット




中2理科 発熱反応と吸熱反応の要点まとめノート 中学生勉強サイトあかね先生




カイロはどうして温かくなるの 酸化反応 の原理を解説




18 号 蓄熱方法及び蓄熱装置 Astamuse




化学平衡の法則とルシャトリエの原理 理系ラボ



発熱 反応 吸熱 反応




反応熱では少数派 吸熱反応 を元塾講師が解説 ページ 2 3 Study Z ドラゴン桜と学ぶwebマガジン




5章 6章の復習 外界と系 孤立系 閉じた系 開いた系 熱化学反応 発熱反応 吸熱反応 熱力学第一法則 エンタルピー 水素結合 Ppt Download




化学反応式 を書く方法について考え




スキルアップ 危険物乙4 化学反応式と熱化学方程式 第33回 サブログ




Ya Af Descubre Como Resolverlo En Qanda




09 0473号 ケミカルヒートポンプ Astamuse
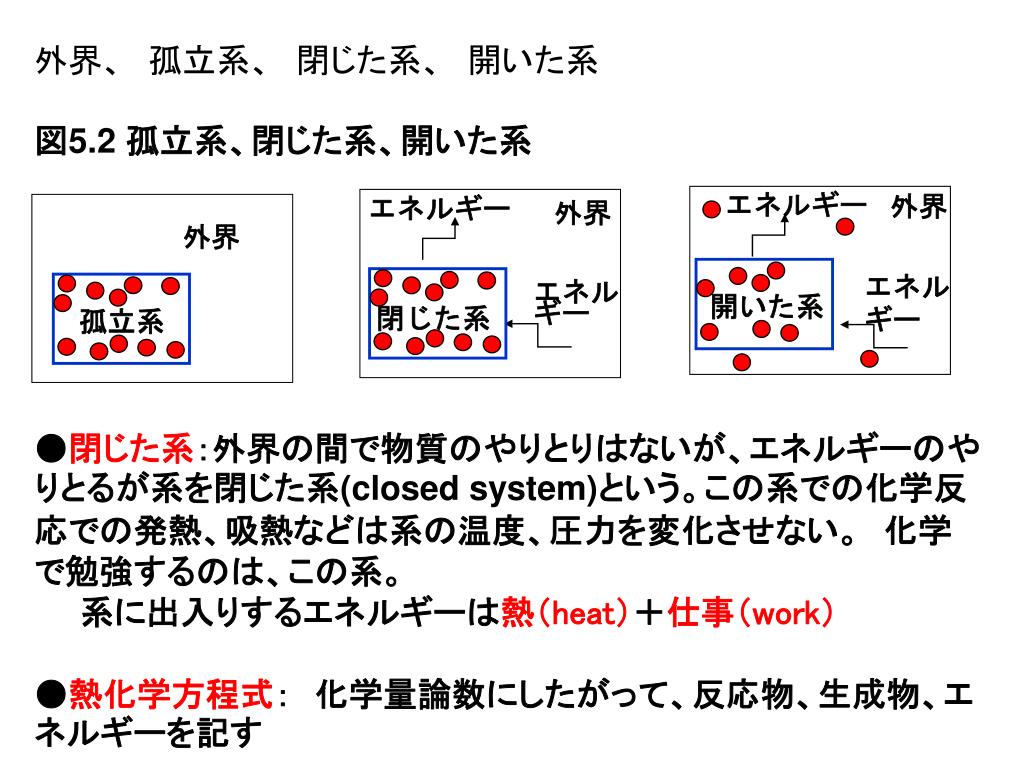



Ppt 5章 6章の復習 外界と系 孤立系 閉じた系 開いた系 熱化学反応 発熱反応 吸熱反応 熱力学第一法則 エンタルピー 水素結合 ブレーンシュテッド酸塩基 ルイス酸塩基 Powerpoint Presentation Id




夕凪亭別館 写真館 化学反応と熱




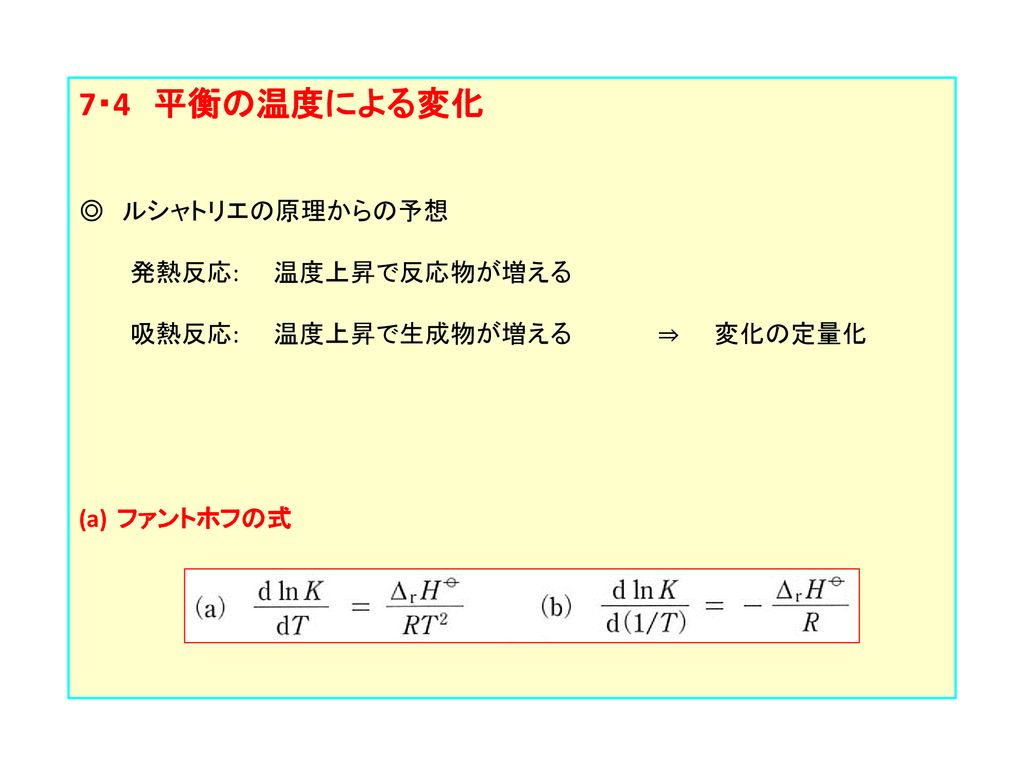
高校化学 ルシャトリエの原理と温度 映像授業のtry It トライイット




液体になると冷える 冷却パックとラムネの意外な共通点 すごい技術 毎日が発見ネット




Nah H2o 2cao 2ca Descubre Como Resolverlo En Qanda




Quimica 化学専門オンライン予備校 化学 物質の三態 状態変化の熱の出入り




09 0473号 ケミカルヒートポンプ Astamuse




Ya Af Descubre Como Resolverlo En Qanda




中2理科 発熱反応 吸熱反応 と 質量保存の法則 の重要ポイントをピックアップし 勉強方法を紹介 札幌市 西区 琴似 発寒 学習塾 個別指導塾 マナビバ
/glowsticks-182836423-5c8efb2746e0fb000172f059.jpg)



グロースティック 吸熱または発熱




3 1tabc Hkh Left 1right Lihat Cara Penyelesaian Di Qanda




反応熱の計算 生成熱 燃焼熱 溶解熱 中和熱 結合エネルギー 理系ラボ




熱化学 化学反応における熱の出入りを把握しよう 図解でわかる危険物取扱者講座




中2 理科 中2 14 化学変化と熱 Youtube




Ppt 教養の化学 Powerpoint Presentation Free Download Id




今後の予定 日程変更あり 5日目 10月21日 木 小テスト 4日目までの内容 小テスト答え合わせ 質問への回答 前回の復習 Ppt Download




5章 6章の復習 外界と系 孤立系 閉じた系 開いた系 熱化学反応 発熱反応 吸熱反応 熱力学第一法則 エンタルピー 水素結合 Ppt Download




16 反応熱と熱化学方程式 Youtube




中2理科 化学変化と温度変化 練習編1 映像授業のtry It トライイット




高校化学 ルシャトリエの原理と温度 映像授業のtry It トライイット



No comments:
Post a Comment